Entfernung von Magnetkügelchen
Entfernung von Magnet-Beads aus Proben nach der Probenvorbereitung mit Einzeltopf und Festphasenverstärkung (SP3).

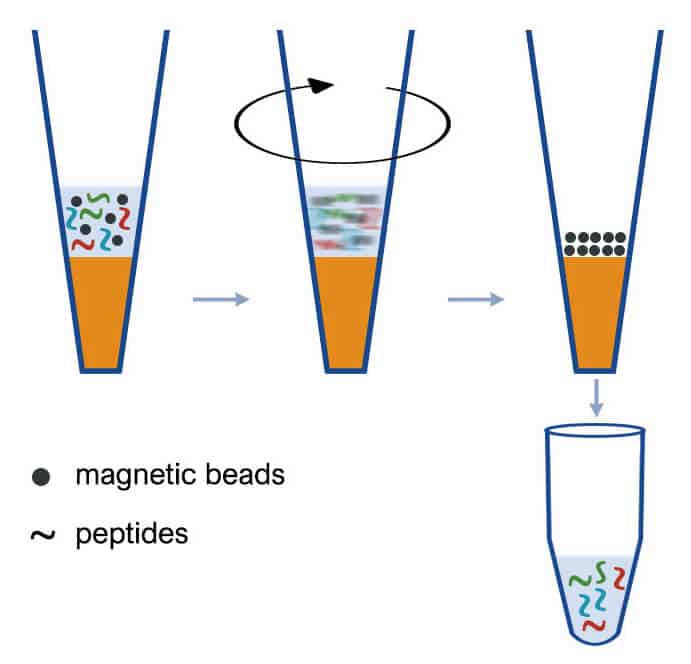
BioSPE® zur Entfernung magnetischer Beads (BeadRem) wird verwendet, um magnetische Beads, die nach dem SP3-Verfahren in Peptid- oder Proteinproben verbleiben und die chromatographische Säule während der LC-MS/MS-Analyse verstopfen könnten, einfach und schnell herauszufiltern.
BioSPE® BeadRem ist in zwei verschiedenen Versionen erhältlich, abhängig von der Art Ihrer Probe:
BioSPE® BeadRem Aqua für wässrige Proben
BioSPE® BeadRem Orga für Proben, die organische Lösungsmittel enthalten
Das BioSPE® Kit besteht aus:
- Filtrationssäulen
- Adaptern (für die Zentrifugation von Spitzen) und/oder Sammelwerkzeugen (Zentrifugenröhrchen oder Sammelplatten). Jedes Kit enthält ein Sammelwerkzeug zum Sammeln von Peptiden/Proteinen im Durchfluss
- Ein detailliertes Protokoll für die schnelle und effiziente Entfernung der Beads und die Rückgewinnung der Peptide/Proteine
Welches Format am besten für Ihre Bedürfnisse geeignet ist, entnehmen Sie bitte der Tabelle auf der Registerkarte „Formate„.
- Effiziente Entfernung von magnetischen Beads mit einem Durchmesser von nur 1µm
- Schneller und einfacher 3-Schritt-Durchlaufprozess
- Möglichkeit, nicht magnetische Beads wie Agarose-Beads herauszufiltern
- Hohe Peptid-/Proteinrückgewinnung
- Keine Lagerungsbeschränkungen (trockene Lagerung bei Raumtemperatur)
- Verschiedene Formate zur Anpassung an Probenvolumen und Durchsatz (StageTips, Spin-Säulen, 96-Well-Platten und SPE-Kartuschen)
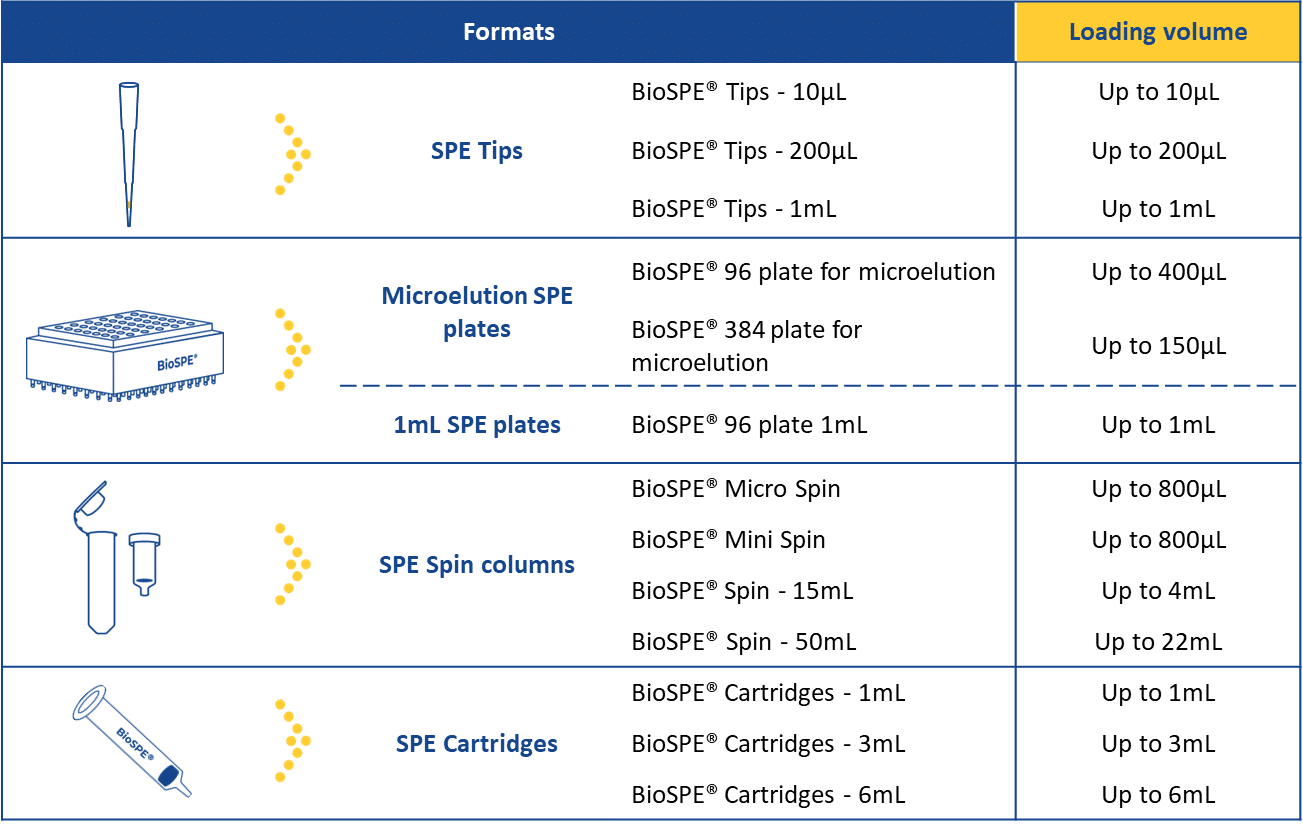
Details zu den Beladungsvolumina unserer verschiedenen BioSPE® BeadRem-Produkte, um je nach Probenvolumen das beste Produkt zu finden.

Peptidentsalzung
Reinigung und Entsalzung von Peptiden in Bottom-up-Proteomik-Ansätzen mit BioSPE® PurePep.

Fraktionierung von Peptiden
Verbesserung der Proteinidentifikation durch LC-MS/MS in komplexen biologischen Proben wie Plasma durch Peptidfraktionierung bei basischem pH.

Aufreinigung von intakten Proteinen
Reinigung intakter Proteine bei Top-down-Proteomik-Ansätzen.

